健診
健診は毎年真面目に受けてきました.特に上部消化管は要注意の体です.アルコールの遺伝子検査ではアルデヒドの分解が悪いDタイプで飲酒による食道がんリスクが高く,ピロリ菌で弱った胃は胃がんのリスクが高いのです.それで胃の健診は毎年内視鏡検査を受けることにしていました.また大腸の健診は50歳ころに便潜血が陽性で大腸ポリープ切除,その後も3-5年おきに大腸内視鏡検査は受けています. また,喫煙者だったので50歳以降毎年胸部のCT検査を受けていました.
内視鏡検査
2021年春,勤務先の病院ではコロナに対する感染防止対策のため,胃カメラの検査数を減らすしかなく,職員が健診で受けられる胃カメラの枠は無くなりました.ピロリ菌除菌以来毎年胃カメラを受けることにしていたので,消化器内科に依頼して保険診療で胃カメラを受けました.胃カメラの画像はモニターで見せてもらいながら検査を受けたので自分の食道がん発見の瞬間を見てしまいました.食道粘膜の表面を這うように広がるタイプでサイズは約6㎝と大きいけど一応早期がん,2つに分かれている部分をまとめて切除する方法で,何とか内視鏡切除できそうとの説明を受けました.
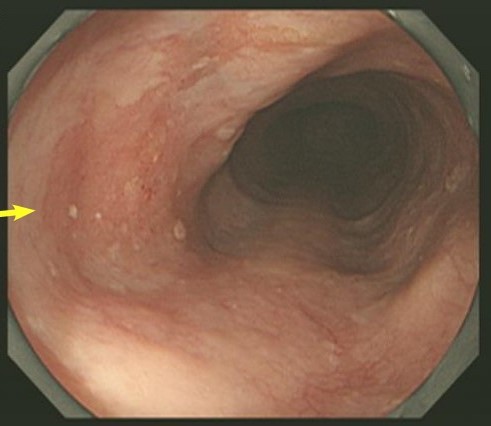
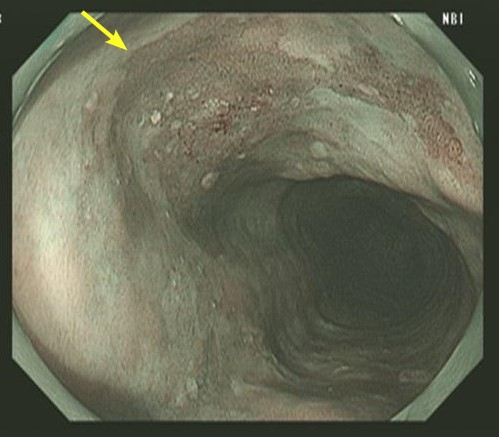
病変は平坦で腫瘤を形成していないものの,周囲とは明らかに色調や表面の不整な性状が違っていて,普通の観察で認識できる病変でした.もっと小さく,表面の変化が少ない病変でも,特殊な光で消化管内部を観察できるようになり(NBI),早期がんの診断能力は随分向上しました.また,古典的な検査としてはヨード散布法があります.正常の食道はヨードに染まり散布すると褐色になるのですが,がんは染まらないので,白っぽく見えます.切除範囲の決定に重要な情報を得られます.
NBIとはNarrow Band Imagingの略で、青と緑の光で消化管粘膜を観察する方法です.日本語にすると狭帯域光観察となります.がんは異常な発育をしており,がんに栄養を供給する毛細血管が拡張や蛇行など異常をきたします.青と緑の狭帯域光で観察すると毛細血管が強調されて粘膜の深い所まで毛細血管が観察でき,深達度も推定できて,食道がんの内視鏡診断の精度が向上しました.
内視鏡治療はどの病院で?
勤務先の内視鏡治療を行っている消化器内科医は優秀な医師で大腸検査や大腸ポリープ切除などでもお世話になっています.食道の病変が小さくて,内視鏡切除だけで済むようならお願いしたいところですが,十分切除しきれない可能性や,治療後の病理検査で根治手術や科化学療法,放射線治療など追加治療が必要な可能性があります.食道がんは増加傾向とは言え,胃がんや大腸がんに比べて数が少なく,多数の症例を扱っている病院は少ないのです.いざ手術になった時には多数の手術経験がある外科チームの存在と,看護師や他のコメディカルの対応が非常に重要です.例えば術前から運動機能を評価して術後に役立てるとか,低下する可能性のある嚥下機能への対応なども含まれます.業界事情にあれこれ詳しい元同僚の外科医に相談し,内視鏡治療医と外科医を推薦してもらって病院をきめました.
内視鏡治療
消化器がんの内視鏡治療はすごく進歩し,表在型の食道がんが発見される頻度が高くなったことと相まって,内視鏡治療で切除ができる病変が増加しました.自分のような6cmくらいに広がったがんは一昔前なら内視鏡での切除は全く無理だったのですが,機器と技術が進歩して切除可能になりました.ESDと呼ばれます.
ESDは Endoscopic Submucosal Dissection の略で日本語では内視鏡的粘膜下層剥離術といいます.病変部の下や周りに薬剤を注入して浮かせて電気メスで切除します.もちろん深部に到達していないがんが対象です.初めて見た時には随分驚きました.当初は随分時間もかかり全身麻酔下とはいえ治療を受ける方も治療をする方も大変だなという印象を持ちましたが,道具も技も進歩し自分のような難しいケースでも名人が行ったとはいえ2時間以内で切除できたようですごいと思いました.ESDは全国的に行われるようになってから20年くらい経過し,標準治療となりました.
PET-CT
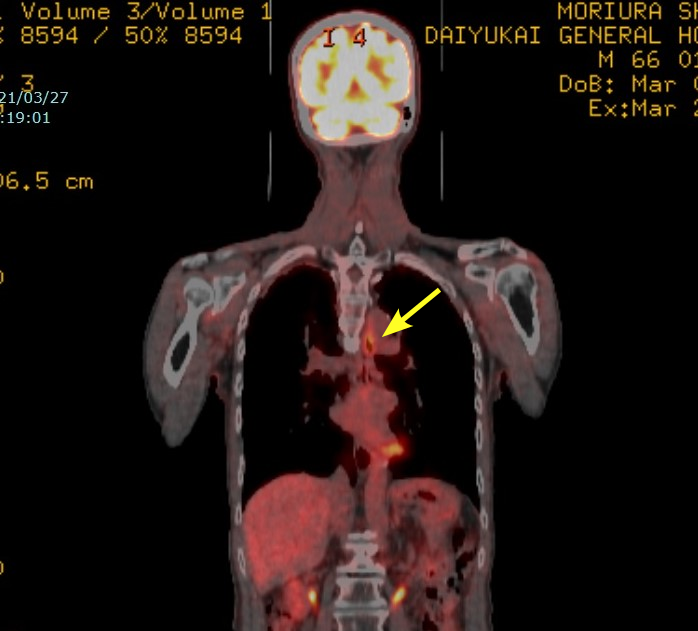
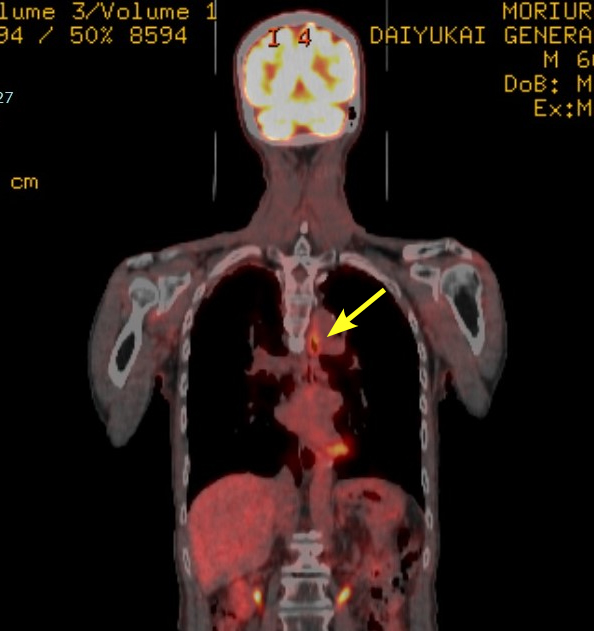
PETとは、Positron Emission Tomography (陽電子放出断層影)の略で,病変の位置を明確にするためにCTを重ねて撮影したものがPET-CTです.PET検査はブドウ糖そっくりの放射性物質(FDG)を注射して体のどこに集まるか(集積)を検査します.がんは増殖が盛んなのでエネルギー源のブドウ糖をたくさん使っていることが多く,ブドウ糖をたくさん取り込みます.FDGもブドウ糖と同じよう病変部に取り込まれるので,それを撮影して診断します.また手術後や感染など炎症部位にも集積します.右の写真では内視鏡治療を受けた部位にFDGの異常な集積が認められます.
PET検査の利点は広範囲の検査が一度にできるので,リンパ節転移や遠隔転移を描出でき,がんの進展を評価できることです.遠隔転移を認めずほっとしたわけですが,根治手術後に判明したリンパ節転移は小さくて診断できなかったようです.
病理検査で追加治療が必要
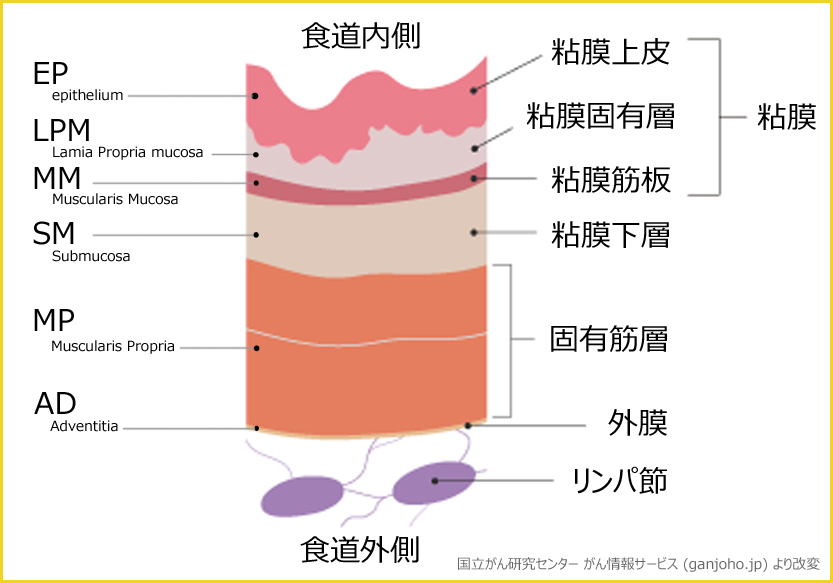
病理検査とは病変を顕微鏡で観察して診断する検査です.切除してもらった標本の重量は数グラム程度と思われますが,リンパ管内にがん細胞を認め(リンパ管浸潤),切除断端もきりきりで,内視鏡治療のみでは不十分との診断で,追加治療が必要になりました.
食道の壁の厚さは3-4mmと薄いのですが,解剖学的に多層で形成され,がん取り扱い規約の面でも病変の深さ(深達度)が深くなると転移の頻度が増して治療成績が悪化するので,治療成績に基づいて分けられ,SM層などは左図の表記以上に細かく表記されます.自分の病変の深さは左図のMMで,この深さまではリンパ節転移の有無にかかわらず早期がんとされるのですが,MMでもリンパ節転移を伴う可能性は5-10%くらいあります.ちなみにSMだと10-40%にリンパ節転移を認め,規約的にも進行がんとなります.
リンパ管浸潤があるとの所見は,食道周囲や頚部,腹部へのリンパ節に転移している可能性が高いということです.手術前に顕微鏡を覗かせてもらいましたが,リンパ管の中にがん細胞がひしめき合っていました. 細胞の形も正常細胞からかけ離れていて,昨年の内視鏡では病変を認めなかったのにこんなに成長しているので,かなりタチの悪い腫瘍だと推察されます.MMは早期がんに分類されますが,リンパ節転移があるとステージは2期となり5年生存率はおよそ65%,すなわち5年以内に死亡する確率が35%と早期がんと言えないようなデータです.
追加治療の選択
追加治療は根治手術または放射線治療+化学療法(業界用語ではケモラジ)です.2期の食道がんに対する放射線化学療法と根治手術の成績を比較すると、欧米では化学放射線療法と根治手術との治療成績が同等とされています(東京大学医学部 放射線科HP).日本癌治療学会のガイドラインでは一部の報告で手術の方が成績が良いことから 「ステージⅡ,Ⅲ食道癌に対して,手術療法を中心とした治療を行うことを弱く推奨する」 と記載されています.しかし両方の治療成績を直接比較した科学的なデータはなく,ケモラジのほうが体への負担が少なく,手術は命にかかわる重篤な合併症を来す可能性もあり,ケモラジを選択することが多いのです.友人の食道専門医もこちらをすすめました.
しかしケモラジが効かなくてCTなどでリンパ節転移が増大してきたりすると,更に根治手術を追加することになります.放射線療法は現在では照射方法が進歩して副作用が減りましたが,それでも照射部位の組織の障害が起こります.化学療法の副作用は個人差がありますがかなり体力を奪います.ケモラジ後の手術ではそれらのの影響で手術合併症の頻度が高くなり,手術死亡が増え (J Thorac Cardiovas Surg 2009),更につらい手術となります.友人の食道専門医は腕がよく,ケモラジ後のむつかしい症例でも上手に手術している実績があり,表面のデータだけでなく,たくさんの経験から,それでもケモラジをすすめてくれたのです.
ケモラジの治療成績が良好なこととリスクが少ないことはわかります.しかし,化学療法がずいぶん進歩し,放射線治療の副作用が軽減しても,がんの治療を多数行ってきて,がんを確実になくすという点ではやはり手術にはかなわないと思っています.手術のあとでリンパ節転移がなくてケモラジで十分だったかなというのより,ケモラジを選んで後で再発巣が出てくる方が心のダメージは大きい気がします.手術の合併症はそれなりに経験しているだけに手術を受けるのは本当に恐ろしいですが,全く迷いなく,とても主観的ですが,根治手術一択でした.内視鏡医から放射線科でケモラジの説明を聞くかと言われましたが断りました.
コメント